Hofmann-elimináció
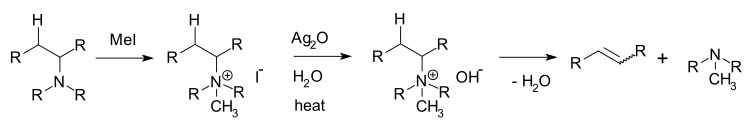
A Hofmann-elimináció aminok eliminációs reakciója, melynek során a legkevésbé stabil (legkevésbé szubsztituált) alkén, a Hofmann-termék keletkezik. Ez ellentétes a Zajcev-szabállyal, mely szerint a szokásos eliminációs reakciók eredményeként a legstabilabb alkén keletkezik. Az elnevezés a reakció felfedezőjére – August Wilhelm von Hofmann – utal.[1][2]
A reakció során az amint metil-jodid feleslegével kvaterner ammónium-jodid sóvá alakítják (kimerítő metilezés), majd ezüst(I)-oxiddal és vízzel kezelve kvaterner ammónium-hidroxid keletkezik. A sót melegítéssel elbontva nagyrészt a Hofmann-termék keletkezik – ennek oka, hogy a távozó csoport sztérikus árnyékoló hatása miatt a hidroxidion a könnyebben hozzáférhető hidrogént fogja lehasítani.
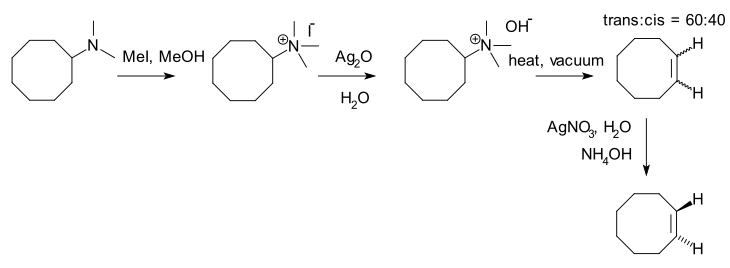
Az egyik példa a transz-ciklooktén szintézise:[3]
Jegyzetek
szerkesztés- ↑ (1851. december 7.) „Researches into the molecular constitution of the organic bases”. Philosophical Transactions of the Royal Society of London 141, 357–398. o. DOI:10.1098/rstl.1851.0017.
- ↑ Aug. Wilh. von Hofmann (1851). „Beiträge zur Kenntniss der flüchtigen organischen Basen” (german nyelven). Annalen der Chemie und Pharmacie 78 (3), 253–286. o. DOI:10.1002/jlac.18510780302.
- ↑ (1973) „trans-Cyclooctene”. Org. Synth..; Coll. Vol. 5: 315
Fordítás
szerkesztésEz a szócikk részben vagy egészben a Hofmann elimination című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.