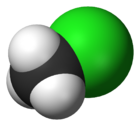
Klórmetán
| Klórmetán | |||
 |
| ||
| IUPAC-név | Klórmetán | ||
| Más nevek | Monoklórmetán, metil-klorid | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 74-87-3 | ||
| PubChem | 6327 | ||
| EINECS-szám | 200-817-4 | ||
| ChEBI | 36014 | ||
| RTECS szám | PA6300000 | ||
| |||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | CH3Cl | ||
| Moláris tömeg | 50,49 g/mol | ||
| Megjelenés | Színtelen, édeskés szagú gáz | ||
| Sűrűség | 2,3065 g/l (gázként, normálállapotban: 0 °C, 1013 mbar nyomás)[1] 1,003 kg/l (folyadékfázis, forrásponton)[1] | ||
| Olvadáspont | −97,4 °C[1] | ||
| Forráspont | -23,76 °C[1] | ||
| Oldhatóság (vízben) | 5 g/l, 20 °C[1] | ||
| Gőznyomás | 4,896 bar (20 °C) 6,6 bar (30 °C) 10,9 bar (50 °C)[1] | ||
| Megoszlási hányados | 0,91 | ||
| Kristályszerkezet | |||
| Molekulaforma | Tetraéderes | ||
| Veszélyek | |||
| EU osztályozás | Nagyon gyúlékony (F+), Ártalmas (Xn), rákkeltő (Cat. 3)[1] | ||
| NFPA 704 | |||
| R mondatok | R12, R40, R48/20[1] | ||
| S mondatok | (S2), S9, S16, S33[1] | ||
| Lobbanáspont | -46 °C | ||
| Öngyulladási hőmérséklet | 625 °C | ||
| LD50 | 1800 mg/kg (patkány, szájon át) LC50: 5,3 mg/l/4 h (inhaláció, patkány)[1] | ||
| Rokon vegyületek | |||
| Rokon vegyületek | Metán Diklórmetán Kloroform Szén-tetraklorid Fluormetán Brómmetán Jódmetán | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A klórmetán vagy metil-klorid a metán klórtartalmú származéka, a halogénezett szénhidrogének közé tartozik. Szobahőmérsékleten színtelen gáz, kissé édeskés szaga van. Könnyen cseppfolyósítható. Csak kis mértékben oldódik vízben, de jól oldható alkoholban és kloroformban.
Kémiai tulajdonságai
szerkesztésGyúlékony gáz. Ha meggyújtják zöldes szélű lánggal ég. Az égéstermékei a víz, a szén-dioxid és a hidrogén-klorid.
Élettani hatása
szerkesztésA metil-klorid mérgező hatású. Ha hosszabb ideig lélegzik be, akkor aluszékonyságot és látási zavarokat okozhat. Mérgezés esetén a betegen oxigénbelélegeztetést kell alkalmazni.
Előállítása
szerkesztésA klórmetán előállítható metanolból sósavval:
Gyártják metánból is katalizátor jelenlétében végzett klórozással is. Körülbelül 90%-os termeléssel állítható elő klórmetán metán és klórgáz 9:1 arányú elegyéből, ha cérium-kloridot is tartalmazó, 450 °C-ra melegített réz(II)-klorid kontakton vezetik át.
Laboratóriumban előállítható enyhén melegített konyhasóoldatba dimetil-szulfát csepegtetésével is.
Felhasználása
szerkesztésMetilezőszerként használják (metilcsoport beépítésére O, S, N, C atomokra). Erre a célra azért nem a legalkalmasabb, mivel kisebb a reakciókészsége, mint a brómmetáné vagy a jódmetáné, illetve gáz halmazállapota miatt körülményes vele dolgozni. Elsősorban a festékiparban, egyes purinok szintézisekor és metil-cellulóz előállítására alkalmazzák. Korábban hűtőgépekben is alkalmazták, ma már toxicitása miatt erre nem használják. Felhasználják műanyagok, szilikonok előállítására is.
Források
szerkesztés- Erdey-Grúz Tibor: Vegyszerismeret
- Bruckner Győző: Szerves kémia, I/1-es kötet
- Kovács Kálmán, Halmos Miklós: A szerves kémia alapjai
