Nitrát-észter
A nitrát-észter az RONO2 képletű szerves funkciós csoport, ahol R tetszőleges szerves csoportot jelöl. A nitrát-észterek a salétromsav és alkoholok észterei. Az egyik közismert példa a nitroglicerin, amely – nevével ellentétben – nem nitrovegyület.
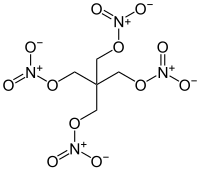
A pentaeritrit-tetranitrát négy nitrát-észter csoportot tartalmazó fontos ipari robbanószer.
Előállítása és reakciói
szerkesztésA nitrát-észtereket jellemzően salétromsav és alkohol kondenzációs reakciójával állítják elő:[1] A legegyszerűbb nitrát-észter, a metil-nitrát metanol és salétromsav reakciójában keletkezik, kénsav jelenlétében:[2]
- CH3OH + HNO3 → CH3ONO2 + H2O
Ezt a fajta kondenzációs reakciót „nitroxilálásnak” is nevezik.
Robbanóképesség
szerkesztésA nitrát-észterek hőbomlása során főként gázok – molekuláris nitrogén (N2) és szén-dioxid – keletkeznek. A robbanás jelentős kémiai energiáját a nitrogénmolekulában levő erős kötés okozza. A nitroglicerin robbanásának egyenlete:
Jól példázza egyes szerves nitrátok rendkívüli érzékenységét a Si(CH2ONO2)4.[3][4] Ennek a vegyületnek egyetlen kristálya is már egy teflonspatulával történő érintés hatására felrobban, így alapos tanulmányozása nem is lehetséges. Exoterm bomlásához (sokkal biztonságosabb in silico kísérlet alapján) hozzájárul, hogy kristályrácsában a szilícium két oxigén nitrito csoporthoz is tud koordinálódni a négy szénatomhoz történő szokásos koordináción kívül. Ez a fajta koordináció elősegíti a szilícium-dioxid (az egyik bomlástermék) keletkezését.
Gyógyászati alkalmazása
szerkesztésAz izoszorbid-dinitrát (Isordil) és az izoszorbid-mononitrát (Imdur, Ismo, Monoket) nitrát-észterek a szervezetben nitrogén-monoxiddá alakulnak, mely erős természetes értágító. Az orvostudomány ezeket az észtereket az angina pectoris kezelésére használja.
Fordítás
szerkesztésEz a szócikk részben vagy egészben a Nitrate ester című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.
Jegyzetek
szerkesztés- ↑ Snyder, H. R.; Handrick, R. G.; Brooks, L. A. (1942). „Imidazole”. Org. Synth..; Coll. Vol. 3: 471
- ↑ Alvin P. Black and Frank H. Babers. „Methyl nitrate”. Org. Synth..; Coll. Vol. 2: 412
- ↑ The Sila-Explosives Si(CH2N3)4 and Si(CH2ONO2)4: Silicon Analogues of the Common Explosives Pentaerythrityl Tetraazide, C(CH2N3)4, and Pentaerythritol Tetranitrate, C(CH2ONO2)4 Thomas M. Klapötke, Burkhard Krumm, Rainer Ilg, Dennis Troegel, and Reinhold Tacke J. Am. Chem. Soc.; 2007 doi:10.1021/ja071299p
- ↑ Sila-Explosives Offer A Better Bang Stephen K. Ritter Chemical & Engineering News May 7 2007Link
