Szerin
| Szerin | |||
| |||

| |||
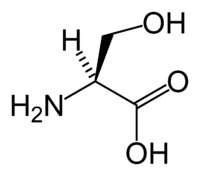
| IUPAC-név | (S)-2-amino-3-hidroxipropánsav | ||
| Kémiai azonosítók | |||
|---|---|---|---|
| CAS-szám | 56-45-1 | ||
| PubChem | 617 | ||
| Gyógyszer szabadnév | serine | ||
| Gyógyszerkönyvi név | Serinum | ||
| |||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C3H7NO3 | ||
| Moláris tömeg | 105,09 g/mol | ||
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |||
A szerin (Ser vagy S)[1] egyike a 22 fehérjealkotó aminosavnak. HO2CCH(NH2)CH2OH.
Kodonjai az UCU, UCC, UCA, UCG, AGU és az AGC. A természetben csak az L-térizomer fordul elő. Számos fehérje felépítésében részt vesz. Nem esszenciális aminosav, vagyis az emberi szervezetben szintetizálódni képes más metabolitokból (pl. glicin).
A selyem fehérjéi különösen gazdagok szerinben (a benne található aminosavak 16%-át teszi ki), innen a neve is (latin sericum=selyem). Először selyemnedvből (sericin) sikerült kivonnia Cramernek 1865-ben. Nagy mennyiségű l-szerint tartalmaz a gyapjú is.
Szerkezetét 1902-ben állapították meg. Első, szerkezetbizonyító szintézisét E. Fischer és Leuchs végezte, a szintézisnél a kiindulási anyag glikolaldehid volt. Hidroxilcsoportja miatt poláris aminosav.
Szerepe
szerkesztésA szerin fontos szerepet játszik az anyagcserében, mivel részt vesz a purinok és a pirimidinek bioszintézisében. Számos aminosav prekurzora, köztük a glicin, cisztein, triptofán aminosavak. Számos más metabolit, például a szfingolipidek prekurzora is. A szerin a folsav előanyaga is, amely a bioszintetikus reakciókban az elsődleges egyszenes csoport-donor.
Jegyzetek
szerkesztés- ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature: Nomenclature and Symbolism for Amino Acids and Peptides. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. (Hozzáférés: 2007. május 17.)